Спектрохимический ряд лигандов
Сравнение расщепляющей способности лигандов в комплексных соединениях
Спектрохимический ряд лигандов представляет собой экспериментально (спектрохимически) полученный ряд, в котором лиганды расположены слева направо по увеличению величины расщепления октаэдрическим полем Δo в октаэдрических комплексах.
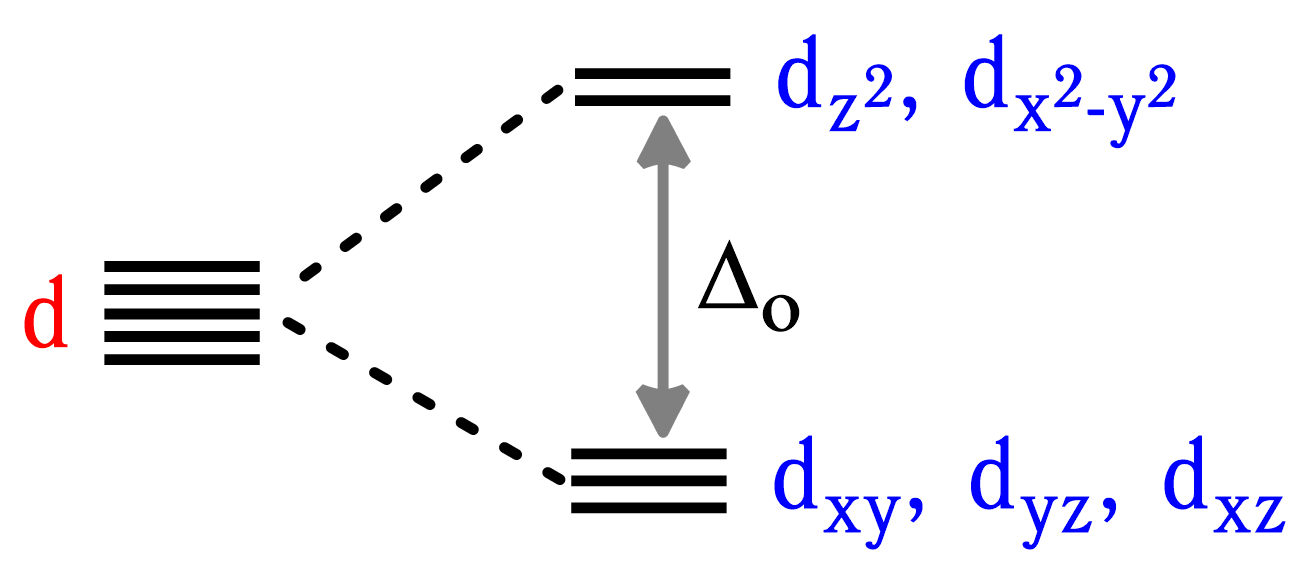
В октаэдрическом поле 5 изначально одинаковых по энергии (вырожденных) d-орбиталей расходятся по энергии из-за разного отталкивания орбиталей различных форм от шести лигандов, и величина этого расщепления Δo увеличивается при движении слева направо по спектрохимическому ряду.
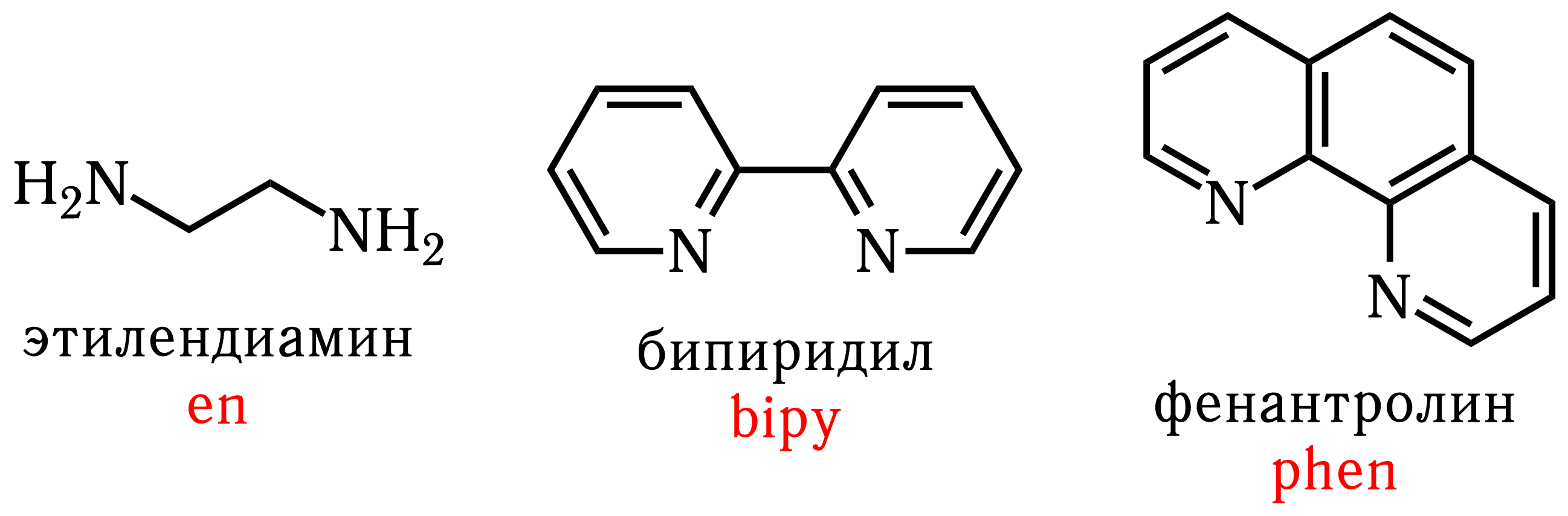
Лиганды до NH3 принято считать лигандами слабого поля, после NH3 — лигандами сильного поля. Граничный аммин-лиганд (NH3) иногда называют лигандом среднего поля, но такое наименование не общепринято. Обратите внимание, что роданид-ион (–SCN—, связывание по атому серы) является лигандом слабого поля, в то время как тиоцианат-ион (–NCS—, связывание по атому азота) — среднего поля. Для удобства тот атом, через который происходит связывание с центральным ионом, выделен в ряду полужирным шрифтом и розовым цветом.
Ряд можно прокручивать влево на мобильных устройствах:

- Увеличение Δo
Физическая химия

Ваше сообщение будет рассмотрено Руководством ChemToday в течение двух дней после отправки и необходимые изменения будут внесены в сайт проекта.
Спасибо за содействие развитию химического портала ChemToday!