Также называется реакцией Назарова. Это реакция, которая была открыта в Институте органической химии (ИОХ) РАН академиком Иваном Николаевичем Назаровым в 1941 году.

Иван Николаевич Назаров, читать подробнее 
ИОХ РАН им. Н. Д. Зелинского
Реакция протекает с нециклическими (не содержащими цикла, в составе которого есть кетонная группа, как, например, в циклогексаноне) кетонами, содержащими α,β- и α’,β’-двойные связи, то есть дивинилкетонами, например, следующими:

Реакция перегруппировки Назарова протекает под действием сильной кислоты Льюиса или Бренстеда (например, H+, AlCl3, FeCl3, BF3*Et2O и так далее), способной присоединиться к кетону по донорно-акцепторной связи. Итак, внимательно смотрим за стрелочками:
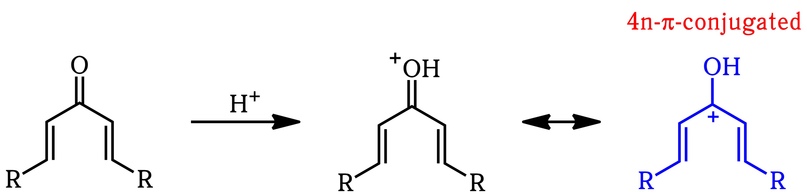
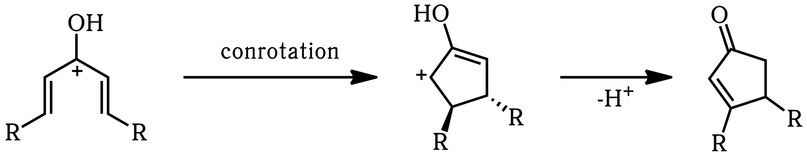
В результате протонирования кетона образуется 4n-сопряжённая π-система, которая может испытывать конротационное замыкание цикла (подробнее об электроциклических реакциях тут):
В результате образуется производное циклопентенона (циклического кетона с пятичленным циклом из атомов углерода с одной двойной связью, сопряжённой со связью C=O). Однако какая региохимия у этой реакции?
Региохимия перегруппировки
Очевидно, что если с одной стороны двойная связь будет более устойчива (то есть сопряжена, например), то этот продукт и будет доминирующим. Приведём следующий пример, где образующаяся двойная связь сопряжена с фенильной группой (Ph-):

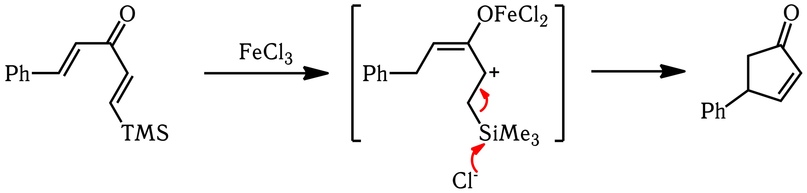
Кремний-направленные реакции. Если в качестве одного из заместителей двойных связей есть силильные группы, то по механизму реакция пойдёт следующим образом: